RÉPONSE RAPIDE,
 Depuis les années 70, l’oxymètre de pouls (PO) permet une évaluation continue non invasive de l’oxygénation du sang artériel, ainsi que la fréquence du pouls. L’estimation du pouls est dérivée de la forme d’ondes pléthysmographiques et sert de mesure indirecte de la perfusion pulsatile. L’alarme sonore assure la surveillance de la fréquence et du rythme cardiaques pendant que le médecin au chevet du patient s’occupe de diverses tâches, avec une tonalité de hauteur variable pour refléter la saturation en oxygène. La surveillance de la fréquence du pouls par oxymétrie offre une autre source d’information, étant donné que les interférences peuvent entraîner un manque de fiabilité du monitorage de la fréquence par ECG. L’utilité globale de la surveillance par PO est incontestable, mais la technologie sous-jacente est complexe. En fonction des caractéristiques d’absorption différentielle de l’oxyhémoglobine et de la désoxyhémoglobine et des pulsations artérielles, de nombreux facteurs peuvent interférer avec la mesure du PO et il faut un traitement complet des signaux pour obtenir des informations utiles. Ce rapport met l’accent sur des scénarios cliniques où la mesure de la fréquence du PO et le signal sonore associé n’ont pas changé convenablement, malgré des pulsations artérielles considérablement altérées.
Depuis les années 70, l’oxymètre de pouls (PO) permet une évaluation continue non invasive de l’oxygénation du sang artériel, ainsi que la fréquence du pouls. L’estimation du pouls est dérivée de la forme d’ondes pléthysmographiques et sert de mesure indirecte de la perfusion pulsatile. L’alarme sonore assure la surveillance de la fréquence et du rythme cardiaques pendant que le médecin au chevet du patient s’occupe de diverses tâches, avec une tonalité de hauteur variable pour refléter la saturation en oxygène. La surveillance de la fréquence du pouls par oxymétrie offre une autre source d’information, étant donné que les interférences peuvent entraîner un manque de fiabilité du monitorage de la fréquence par ECG. L’utilité globale de la surveillance par PO est incontestable, mais la technologie sous-jacente est complexe. En fonction des caractéristiques d’absorption différentielle de l’oxyhémoglobine et de la désoxyhémoglobine et des pulsations artérielles, de nombreux facteurs peuvent interférer avec la mesure du PO et il faut un traitement complet des signaux pour obtenir des informations utiles. Ce rapport met l’accent sur des scénarios cliniques où la mesure de la fréquence du PO et le signal sonore associé n’ont pas changé convenablement, malgré des pulsations artérielles considérablement altérées.
Les observations rapportées ici sont survenues après une actualisation majeure des moniteurs au chevet des patients dans notre centre. La première observation est survenue chez des patients avec un pontage cardio-pulmonaire (CPB) et la deuxième était avec des patients non-CPB présentant un arythmie mettant leur vie en danger. Notre installation de surveillance est composée d’un oxymètre de pouls Masimo SET (version SpO2 intégré MS:DSP:V05:03.01.08), réglé à 2–4 ou 4–6-données seconde en moyenne avec des capteurs RD SET à sonde optique, appliqués à un doigt (ou l’oreille dans un cas d’asystolie) conformément à la recommandation du fabricant (Masimo Corporation, Irvine, California, USA). Le PO est intégré au monitorage Mindray N1, avec la fréquence du pouls de l’oxymètre réglée comme étant la source principale de représentation audible de la fréquence (Mindray Global, Nanshan, Shenzhen, R.P. Chine). La fonction sonore Smart Tone de l’oxymètre Masimo est activée et ne peut pas être désactivée. Cette fonction est conçue pour maintenir une tonalité variable pendant les conditions où le rapport signal-bruit est faible. Toutefois, dans le cadre d’un CPB, des fréquences de pouls erronées sont indiquées par l’oxymètre chez 50 % au moins de nos patients pendant un pontage, même pendant un clampage de l’aorte. La fréquence indiquée n’était pas liée aux réglages de la pompe du CPB. La Figure 1 montre deux exemples pendant une période d’absence de pulsatilité où l’oxymètre signalait une fréquence de pouls proche de la mesure de référence précédente dans les années 60. La fonction sonore de l’appareil de surveillance a maintenu un rythme régulier et une tonalité stable. Nous avons signalé cette expérience au fabricant et un audit initial mené par la société n’a pas permis d’identifier de quelconques dysfonctionnements. Le mode d’emploi du fabricant précisait que « Le Masimo SET continuera d’indiquer une saturation artérielle en oxygène et une fréquence du pouls exactes en cas de mouvement et de perfusion basse, même si la forme d’ondes pléthysmographiques n’est pas optimale », et que « Il est important de noter que même lorsque « Signal IQ est faible », il est fort probable que la mesure soit correcte ; sinon le système n’afficherait aucune valeur ».1 Dans ce contexte de CPB toutefois, nous suggérons que l’algorithme ne peut pas refléter correctement la fréquence du pouls réelle.
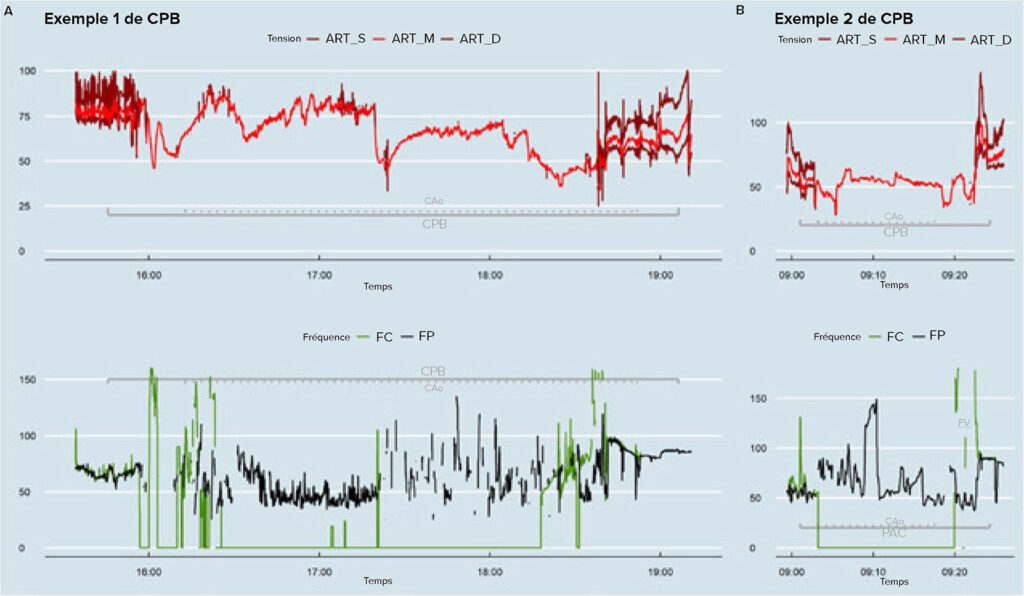
Figure 1 : Pressions artérielles, fréquence cardiaque (FC) dérivée de l’ECG et fréquence de pouls (FP) dérivée de l’oxymètre dans deux cas, pendant un pontage cardio-pulmonaire (CPB) et un clampage de l’aorte (AoX). Remarque : la détection de la FP se poursuit également pendant la fibrillation ventriculaire (FV) après le déclampage.
La deuxième observation concernait des patients présentant une arythmie mettant leur vie en danger, où la mesure de la fréquence du pouls de l’oxymètre Masimo indiquait faussement une fréquence et un rythme cardiaques stables. Nous l’avons remarqué chez un patient qui soudainement a développé une fibrillation ventriculaire (FV) une fois un CPB terminé et chez deux patients en bradycardie extrême. La FV est survenue après un CPB pour un remplacement valvulaire aortique, pendant l’hémostase chirurgicale, avec le sternum encore ouvert (Figure 2, graphique gauche). Le faible débit cardiaque en résultant a été mis en évidence par l’hypotension et une chute du dioxyde de carbone télo-expiratoire. Au bout de 23 secondes, une défibrillation réussie a rétabli les paramètres hémodynamiques.
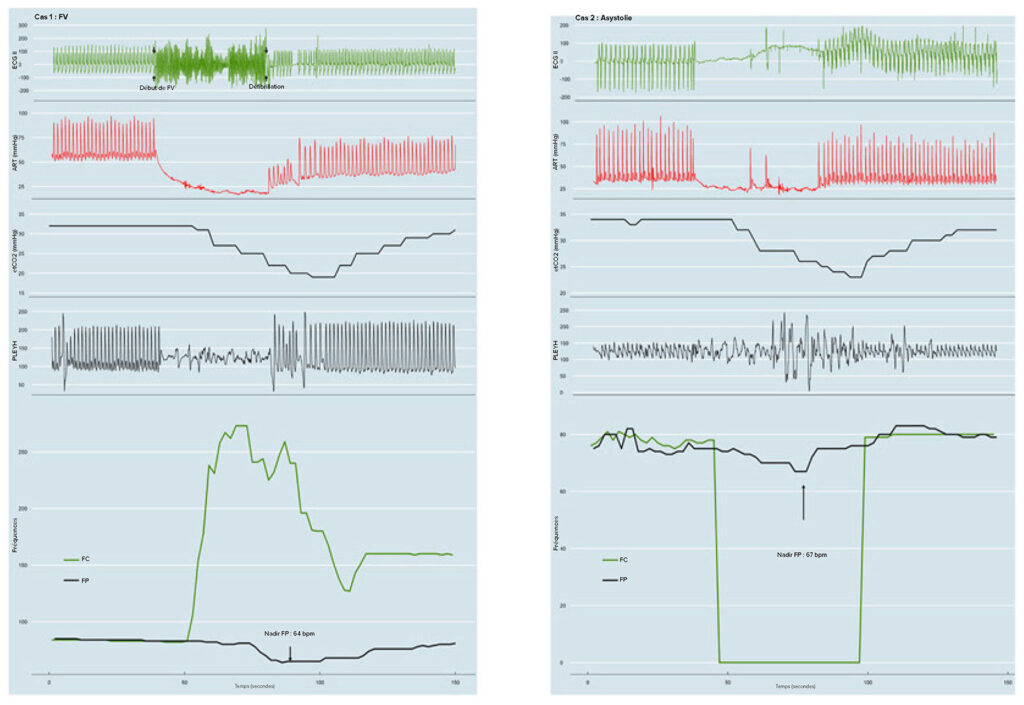
Figure 2 : Données de l’ECG, de la pression artérielle, de la capnographie de fin d’expiration et de l’oxymétrie, ainsi que la fréquence cardiaque (FC) dérivée de l’ECG et la fréquence de pouls (FP) dérivée de l’oxymètre. Début soudain de fibrillation ventriculaire (gauche) et asystolie aiguë (droite) avec effets hémodynamiques, sans effet significatif sur la mesure de la fréquence du pouls par oxymétrie.
Peu après le début de la FV, des oscillations erratiques ont été capturées par le capteur de l’oxymètre qui n’existaient pas avant ou après la FV et la défibrillation qui y a fait suite, alors que le patient était allongé et immobile, sans que le doigt du patient ou l’oxymètre ne soit soumis à un quelconque mouvement externe majeur. Pendant cet épisode, la fréquence du pouls de l’oxymètre a affiché uniquement un déclin modéré 15 secondes après le début de la FV, chutant à 64 battements par minute au bout de 24 secondes. Encore une fois, la tonalité sonore de l’appareil de surveillance Mindray reflétait ce déclin modéré de la fréquence du pouls. Après la défibrillation, les formes d’ondes de l’ECG, la pression artérielle et les formes d’ondes pléthysmographiques indiquaient que la fréquence cardiaque était rétablie à sa fréquence antérieure à la FV. Toutefois, la fréquence cardiaque basée sur l’ECG présentait un double comptage, alors que la fréquence du pouls de l’oxymètre se rétablissait à la fréquence antérieure à la FV.
Dans un cas d’asystolie (Figure 2, graphique droit), les mêmes observations ont été faites. C’était avant le CPB, pendant l’instrumentation du cathéter de la veine jugulaire pour le placement de la canule d’ECMO. La forme d’onde pléthysmographique de l’oxymètre montre un signal oscillatoire erratique peu de temps après le début de l’asystolie. Malgré l’asystolie soudaine avec collapsus hémodynamique, le nadir de la fréquence de pouls avec l’oxymètre a atteint 67 battements par minute. Alors que le pic chutait avec le déclin de la saturation, la tonalité constante de l’alarme sonore ne correspondait pas à l’épisode d’asystolie.
DISCUSSION
L’impact du mouvement du patient et des états de faible perfusion sur la fiabilité des mesures de la saturation est bien connue et une recherche de solutions est en cours.2,3 La fiabilité de la mesure de la fréquence du pouls par oxymètre, toutefois, fait trop rarement l’objet d’études, en particulier pendant des états de pulsatilité faible et inexistante et lorsque la tonalité de l’alarme sonore n’est pas affectée. Les comparaisons entre le PO et la fréquence cardiaque de l’ECG ont été réalisées principalement dans le cadre des soins néonatals, où on sait que l’oxymétrie de pouls sous-estime la fréquence cardiaque dans les premières minutes après l’accouchement.4 Les études signalent 35 % de fausses mesures de bradycardie5 et une sensibilité globale de (seulement) 89 % pour la détection d’une fréquence cardiaque inférieure à 100 battements par minute.6
Nous avons signalé nos observations et nos inquiétudes quant aux conséquences cliniques aux sociétés Masimo et Mindray. Il convient de noter que des observations semblables avaient déjà été rapportées à Masimo à 2007,7. Masimo avait alors ajusté son logiciel pour permettre la désactivation de la fonction Smart Tone. La fonction Smart Tone a été développée à l’origine pour réduire au minimum l’impact des artéfacts liés aux mouvements. Cependant, nous confirmons ici que cet algorithme pourrait aussi être induit en erreur par d’importantes perturbations du rythme. Dans nos appareils de surveillance Mindray actuels toutefois, la fonction Smart Tone est activée en permanence. C’est probablement la cause de la tonalité trompeuse de l’alarme sonore. Les fabricants recherchent une solution à ce problème afin de pouvoir le supprimer dans l’appareil de surveillance Mindray. En attendant, nous restons particulièrement vigilants et dans la mesure du possible, nous ajustons la source de la mesure de la fréquence du pouls en fonction du cathéter artériel. Dans ce contexte, on continue à dériver la hauteur du pouls du signal de l’oxymètre, mais la fréquence de pouls audible est un reflet de la fréquence de pouls réelle.
Michael Vandenheuvel, MD, est médecin anesthésiste du département d’anesthésie et de médecine périopératoire de l’hôpital universitaire de Gand (Belgique).
Patrick Wouters, MD, PhD, est professeur et chef de la recherche du département d’anesthésie et de médecine périopératoire de l’hôpital universitaire de Gand (Belgique).
Luc De Baerdemaeker, MD, PhD, est professeur et chef du département d’anesthésie et de médecine périopératoire de l’hôpital universitaire de Gand (Belgique).
Les auteurs ne signalent aucun conflit d’intérêts.
DOCUMENTS DE RÉFÉRENCE
- Masimo Inc. Masimo Signal I.Q. whitepaper. 2010. www.asa-abstracts.com. Accessed September 4, 2023.
- Louie A, Feiner JR, Bickler PE, et al. Four types of pulse oximeters accurately detect hypoxia during low perfusion and motion. Anesthesiology. 2018;128:520–530. PMID: 29200008.
- Giuliano KK, Bilkovski RN, Beard J, Lamminmäki S. Comparative analysis of signal accuracy of three SpO2 monitors during motion and low perfusion conditions. J Clin Monit Comput. 2023:1–11. PMID: 37266709.
- Anton O, Fernandez R, Rendon-Morales E, et al. Heart rate monitoring in newborn babies: a systematic review. Neonatology. 2019;116:199–210. PMID: 31247620.
- Khoury R, Klinger G, Shir Y, et al. Monitoring oxygen saturation and heart rate during neonatal transition. comparison between two different pulse oximeters and electrocardiography. J Perinatol. 2021;41:885–890. PMID: 33250516.
- Kamlin COF, Dawson JA, O’Donnell CPF, et al. Accuracy of pulse oximetry measurement of heart rate of newborn infants in the delivery room. J Pediatr. 2008;152:756–760. PMID: 18492509.
- Forde RER, DeBros FM, Guimaraes EL, Sandberg WS. Misleading behavior of Masimo pulse oximeter tone during profound bradycardia. Anesthesiology. 2007;107:1038–1039. PMID: 18043086.
Fréquence de pouls mesurée par l’oxymètre de pouls affichée et alarme sonore générée pendant l’absence d’un pouls physiologique – Réponse de Masimo
RÉPONSE :
Masimo a soigneusement étudié le rapport de Vandenheuvel et al. et a identifié d’importantes réflexions à partager avec les lecteurs. Outre la remise du rapport à l’APSF, UZ Gand a contacté Masimo pour signaler des cas où la mesure de la fréquence du pouls (FP) et la tonalité variable associée à la hauteur de la carte Masimo SET dans un appareil de surveillance Mindray n’indiquaient pas la fréquence de pouls réelle, pendant un pontage cardio-pulmonaire (CPB) et dans deux cas non-CPB liés à des arythmies sans pouls (fibrillation ventriculaire [FV] et asystolie). L’oxymètre (PO) utilisé dans le cas d’asystolie (capteur d’oreille RD SET E1), un ensemble de données numériques extraites de l’appareil de surveillance Mindray et les messages d’alarme (voir le graphique du haut de la Figure 3) ont été fournis à Masimo. Des ensembles de données limités de Mindray (mais pas les capteurs) étaient disponibles pour les cas de FV et de CPB. Les tracés des ondes physiologiques en format comprimé fournies dans le rapport à l’APSF ont également été transmis à Masimo.
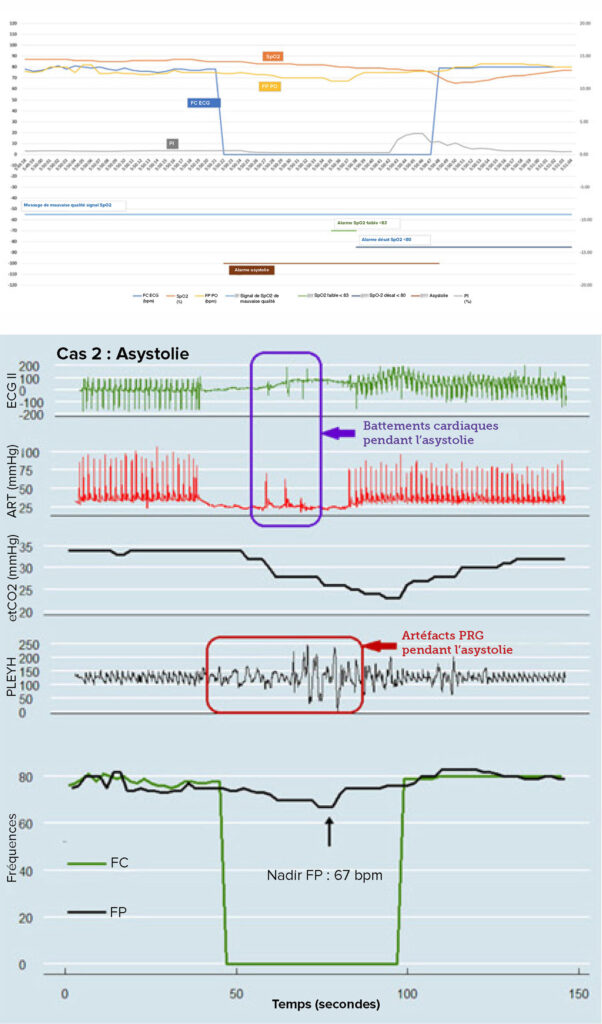
Figure 3 – légende : Premier graphique : Tracés de la SpO2, de la FP dérivée du PO et de la FC dérivée de l’ECG HR ainsi que les messages d’alarmes techniques (description, heure et durée) qui étaient présents pendant le cas d’asystolie. Remarque : le message « !Signal de SpO2 de mauvaise qualité » était affiché pendant la durée totale de l’ensemble des données et l’alarme « !!SpO2 faible <83 » est survenue pendant 13 à 16 secondes après le début de l’épisode d’asystolie, suivie de l’alarme « !!!SpO2 désat <80 », affichée au bout de 16 secondes après le début de l’épisode d’asystolie et qui a continué jusqu’à la fin de l’ensemble de données.
Deuxième graphique : Données du cas d’asystolie de Vandenheuvel et al, annotées avec un rectangle violet pour mettre en évidence les battements du cœur à mi-chemin de l’asystolie (indiqués par des « pics » simultanés dans la forme comprimée des ondes de l’ECG et les pulsations de pression dans le tracé de la ligne artérielle).
Masimo a testé le capteur d’oreille, qui fonctionnait conformément au cahier des charges. Les données relatives aux paramètres et aux alarmes pour le cas d’asystolie ont été comparées aux tracés en format comprimé fournis pour l’ECG, la pression artérielle, EtCO2, SpO2 les formes d’ondes pléthysmographiques (pleth) et les courbes de tendance pour la fréquence cardiaque (FC) basée sur ECG et la FP basée sur la pléthysmographie.
PRINCIPALES CONSTATATIONS :
- D’après l’équipe d’UZ Gand, l’asystolie a débuté avant le CPB, pendant la tentative d’insertion d’un cathéter/d’une canule d’ECMO dans la veine jugulaire et s’est terminée 26 secondes après la fin des efforts.
- Les tracés en format comprimé montrent quelques battements pulsatiles pendant l’épisode d’asystolie sur l’ECG, les formes d’ondes artérielles et pléthysmographiques.
- L’appareil de surveillance Mindray (avec Masimo SET) a affiché un message de signal de SpO2 de mauvaise qualité longtemps avant et après l’épisode. Ce point est important parce qu’une mauvaise qualité de signal peut empêcher des mesures exactes et précises.
- La forme d’ondes pléthysmographiques a enregistré un signal oscillatoire peu de temps après le début de l’asystolie. En raison de la position du capteur du PO sur l’oreille, il est entièrement possible que les actions des médecins, à proximité de la tête, du cou ou de l’oreille, pendant l’insertion et le retrait du cathéter/de la canule d’ECMO, aient causé un mouvement involontaire et l’artéfact en résultant, indiqué dans la forme d’ondes pléthysmographiques qui ont eu une incidence sur les mesures de FP basées sur le PO. L’appareil Masimo SET est conçu pour déclencher une alarme en moins de 8 secondes après le début d’une asystolie en l’absence d’artéfact de mouvement. Il est probable que la reconnaissance opportune de l’épisode d’asystolie par le PO ait été empêchée par l’artéfact oscillatoire dans le signal pléthysmographique et les battements visibles pendant l’asystolie, aussi bien sur l’ECG que dans les tracés artériels (voir l’encadrement violet dans la Figure 3), qui ont eu une incidence sur l’exactitude de l’estimation de la FP.
- Les données de Mindray indiquent une chute de SpO2 de 85 % à 67 % et une alarme de SpO2 faible s’est déclenchée environ 13 secondes après le début de l’asystolie.
UZ Gand n’a pas fourni à Masimo le capteur utilisé dans le cas de FV. Toutefois, ils ont envoyé les tracés des paramètres en format compressé et une donnée du paramètre Hz, mais sans les données des messages d’alarme. Les principales conclusions de cette étude des données sont les suivantes :
- La fibrillation ventriculaire a duré environ 24 secondes et s’est terminée par une défibrillation.
- Les tracés comprimés ne montrent aucun artéfact visible jusqu’à quelques secondes après le début de la FV lorsqu’un signal oscillatoire erratique apparaît sur la pléthysmographie.
- Le signal erratique de pléthysmographie reflète probablement l’artefact de mouvement causé par les médecins pendant la préparation et la réalisation de la défibrillation, car cet artéfact n’était pas présent avant ou après l’épisode de FV.
Il est bien reconnu que les paramètres de la surveillance physiologique ont des caractéristiques uniques en matière de précision, stabilité, fiabilité et caractéristiques confondantes. Par exemple, la FC post-défibrillation dans le cas de FV met l’accent sur la limitation de la surveillance par ECG basée sur le signal. Le tracé de l’ECG montre le retour de la FC à sa fréquence de 78-80 bpm, antérieure à l’épisode de FV. Toutefois, des ondes « T » ou « P » probablement prononcées dans l’ECG post défibrillation ont causé le double comptage de la FC, alors que la FP générée par le PO retournait avec précision à la fréquence antérieure à la FV.
De même, la forme d’ondes pléthysmographiques, qui mesure les changements de densité optique sur le parcours du capteur, est limitée par l’origine du signal. En particulier, en l’absence d’un pouls artériel réel, un signal oscillatoire confondant, qui peut imiter la forme d’une véritable pléthysmographie (induite par les médecins, un mouvement ou un appareil) peut présenter une FP qui n’est pas représentative d’une FC dérivée d’un ECG.
Il est important de noter que la forme d’ondes pléthysmographiques de Masimo reflète le signal brut enregistré par son capteur optique. Par conséquent, la forme du tracé est représentatif d’un réel changement du signal optique. Les algorithmes uniques de traitement du signal de l’appareil Masimo SET sont conçus pour évaluer avec précision la fréquence de pouls et la saturation en oxyhémoglobine pendant un mouvement et une perfusion faible. Cependant, le scénario dans le cas d’asystolie, où il n’y a pas de véritable pression artérielle mais un signal pléthysmographique oscillatoire en raison des facteurs confondants, présente une limite de la technologie de l’oxymétrie en général.
Dans les exemples de CPB, les deux cas présentent une grande variabilité de la pression artérielle moyenne pendant le CPB. Dans le premier cas, la FC dérivée de l’ECG et la FP dérivée du PO sont élevées alors que le cœur ne bat pas. La forme d’ondes pléthysmographiques non physiologiques est probablement due à une petite pression pulsée produite par la pompe du CPB, un phénomène connu de longue date des anesthésistes cardiaques.1 Masimo SET est souvent capable de détecter ces pulsations,1 mais le PO n’est pas fiable pendant un CPB. En fait, Reich et al. ont signalé que le CPB représentait plus de 30 % des cas où les données du PO n’étaient pas fiables pendant au moins 10 minutes.2
Enfin, dans la discussion de Vandenheuvel et al., les auteurs se méprennent en disant que « la fonction Smart Tone a été développée à l’origine pour réduire au minimum l’impact des artéfacts liés aux mouvements. » La fonction SmartTone de Masimo détermine uniquement si la tonalité de hauteur variable est activée pendant des conditions où le rapport signal-bruit est faible. Si la fonction SmartTone est activée, une tonalité reflétant la fréquence de la FP et la hauteur reflétant le pourcentage de SpO2 sera déclenchée. Si la fonction SmartTone est désactivée, aucune tonalité ne sera déclenchée pendant des conditions où le rapport signal-bruit est faible. La capacité à entendre la tonalité de saturation variable et la fréquence de la FP dans des conditions où le rapport signal-bruit est faible est souvent bien reçue dans les domaines de soin où les artéfacts sont courants et où les patients sont observés régulièrement. Elle est moins adaptée aux domaines de soin où ces conditions ne sont pas aussi habituelles.
La fonction SmartTone est un paramètre configurable dans les appareils de surveillance Masimo. Par défaut, ils sont réglés sur « OFF » pour réduire au minimum la possibilité d’activation de la fonction SmartTone sans qu’un utilisateur ne comprenne son fonctionnement et sache comment mettre la fonction SmartTone en et hors service, en fonction des circonstances de son cas d’usage. Toutefois, dans le cadre du déploiement d’appareils de surveillance Mindray, le réglage par défaut de la fonction SmartTone est « ON » (activé) et il est impossible de la désactiver (« OFF »). Suite aux acquis issus de l’expérience à UZ Gand, Mindray a étudié les problèmes cliniques et techniques avec un esprit ouvert. Ils ont convenu de transformer la fonction SmartTone pour qu’elle soit « désactivée » (OFF) par défaut.
Pour résumer, les cas présentés par les médecins de l’UZ Gand fournissent des informations et des avertissements aux médecins à propos des conditions confondantes qui peuvent avoir une incidence sur les mesures de la FP basée sur un PO et de la FC basée sur un ECG. Ils préviennent également de l’inconvénient potentiel dans certaines applications cliniques d’un déploiement unique de la fonction SmartTone dans un appareil de surveillance multiparamètres. Masimo et Mindray utilisent le retour d’information de leurs clients, qui constitue un élément fondamental pour des opportunités potentielles d’amélioration de la satisfaction des utilisateurs de nos produits, comme en témoigne la planification de modification du déploiement de la fonction SmartTone dans les appareils de surveillance Mindray, résultat de la collaboration avec les médecins d’UZ Gand.
Cordialement,
Vikrant Sharma, PhD
vice-président, Optical Sciences, Masimo Corp, Irvine, Californie
Steven J. Barker, PhD, MD
Directeur des affaires scientifiques, Masimo Corp., Irvine, Californie
Rick Fishel
Président, Équipementiers internationaux et développement stratégique des activités, Masimo Corp.,
Irvine, Californie
Daniel Cantillon, MD
Médecin-chef, Masimo Corp., Irvine, Californie
William C. Wilson, MD, MA
vice-président exécutif, Opérations cliniques, Masimo Corp., Irvine, Californie
Déclarations : Vikrant Sharma, Rick Fishel, Daniel Cantillon et William C. Wilson sont des employés à temps plein de Masimo. Steven J. Barker est employé à temps partiel de Masimo.
DOCUMENTS DE RÉFÉRENCE
- Irita K, Kai Y, Akiyoshi K, et al. Performance evaluation of a new pulse oximeter during mild hypothermic cardiopulmonary bypass. Anesth Analg. 2003;96:11–14. PMID: 12505915.
- Reich DL, Timcenko A, Bodian CA, et al. Predictors of pulse oximetry data failure. Anesthesiology.
1996;84:859–64. PMID: 8638840.
Ces informations sont fournies à des fins de formation liée à la sécurité et ne doivent pas être interprétées comme un avis médical ou légal. Les réponses individuelles ou de groupe ne sont que des commentaires fournis à des fins de formation ou de discussion et ne sont ni des déclarations d’avis ni des opinions de l’APSF. Il n’est pas dans l’intention de l’APSF de fournir un avis médical ou légal spécifique ni de se porter garante des points de vue ou recommandations exprimés en réponse aux questions postées. L’APSF ne pourra en aucun cas être tenue responsable, directement ou indirectement, des dommages ou des pertes causés ou présumés avoir été causés par, ou en rapport avec la confiance accordée à, ces informations.


 Issue PDF
Issue PDF